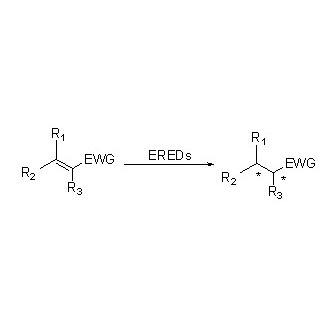
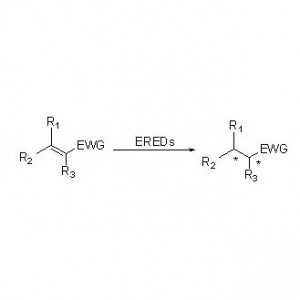
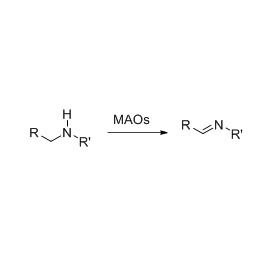
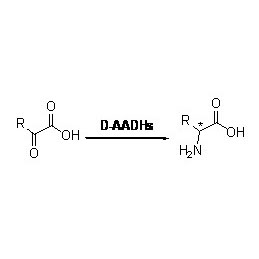
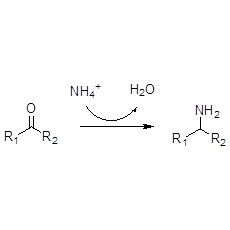
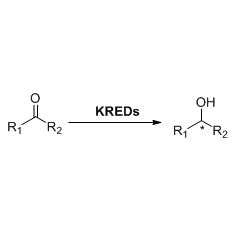
Ene-reductase (ERED)
ES-EREDs katalyseren diverse substraattypen vanwege het brede spectrum aan substraten. Over het algemeen worden de C=C-bindingen van α,β-onverzadigde verbindingen met elektronenabsorberende groepen (waaronder ketonaldehyden, nitrogroepen, carbonzuren, esters, anhydriden, lactonen, iminen, enz.) gemakkelijk gereduceerd door ES-EREDs, maar de niet-geactiveerde dubbele bindingen niet.
SyncoZymes heeft 46 verschillende ERED-enzymproducten ontwikkeld (genummerd van ES-ERED-101 tot en met ES-ERED-146).
Katalytisch mechanisme:
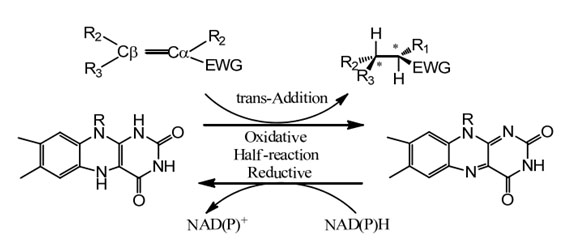
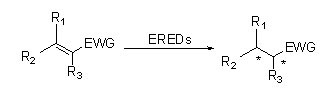
| Enzymen | Productcode | Specificatie |
| Enzympoeder | ES-ERED-101~ ES-ERED-146 | een set van 46 Ene-reductasen, 50 mg per stuk 46 stuks * 50 mg / stuk, of een andere hoeveelheid |
| Screeningkit (SynKit) | ES-ERED-4600 | een set van 46 Ene-reductasen, 50 mg per stuk 46 stuks * 50 mg / stuk, of een andere hoeveelheid |
★ Hoge substraatspecificiteit.
★ Sterke chirale selectiviteit.
★ Hoge conversieratio.
★ Minder bijproducten.
★ Milde reactieomstandigheden.
★ Milieuvriendelijk.
★ Hoge veiligheid.
➢ Normaal gesproken moet het reactiesysteem het volgende bevatten: substraat, bufferoplossing (optimale reactie-pH), co-enzymen (NAD(H) of NADP(H)), een systeem voor co-enzymregeneratie (bijv. glucose en glucosedehydrogenase) en ES-ERED.
➢ Alle ES-EREDs kunnen respectievelijk worden getest in het bovenstaande reactiesysteem of met de ERED Screening Kit (SynKit ERED).
➢ Alle soorten ES-ERED's die overeenkomen met verschillende optimale reactieomstandigheden moeten afzonderlijk worden bestudeerd.
➢ Een hoge concentratie substraat of product kan de activiteit van ES-ERED remmen. Deze remming kan echter worden opgeheven door het substraat in batches toe te voegen.
Voorbeeld 1 (α,β-onverzadigde aldehyden of ketonen)(1):
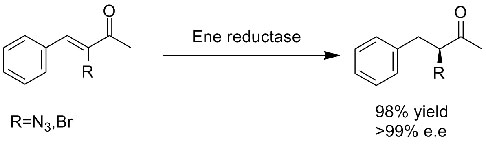
Voorbeeld 2 (α,β-onverzadigde carbonzuren en hun derivaten)(2):
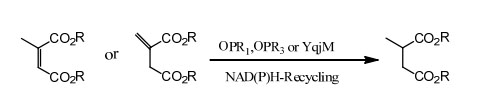
Bewaar gedurende 2 jaar beneden -20℃.
Vermijd contact met extreme omstandigheden zoals hoge temperaturen, hoge/lage pH-waarden en hoge concentraties organische oplosmiddelen.
1. Lucídio C, Fardelone J, Augusto R, e tal. J.Mol.Catal.B:Enzym., 2004, 29: 41-45.
2. Stueckler C, Hall M, Ehammer H, et al. .Org.Lett, 2007, 9(26): 5409-5411.